- Simona Di Filippi, Maria Francesca Zamaro e Sonia Cogo
- Original Article
Gestione infermieristica del paziente settico: monitoraggio e procedure
- 3/2017-Ottobre Supplemento
- ISSN 2532-1285
- https://doi.org/10.23832/ITJEM.2017.030
Simona Di Filippi e coll.
Osservazione e monitoraggio
Nel sospetto di una sepsi, dopo aver rilevato i parametri vitali seguendo il metodo A-B-C-D-E, uno strumento utilizzabile è il q-SOFA, una versione rivista del SOFA score, dove la prima lettera sta a indicare “quick” ovvero “veloce” da usare rapidamente al letto del paziente e che va a indagare tre semplici parametri vitali, ovvero pressione arteriosa, frequenza respiratoria e stato mentale. In caso di almeno due riscontri patologici (es. tachipnea, ipotensione o GCS < 15) il paziente ha un alta probabilità di sepsi e va ricoverato in ambiente idoneo.
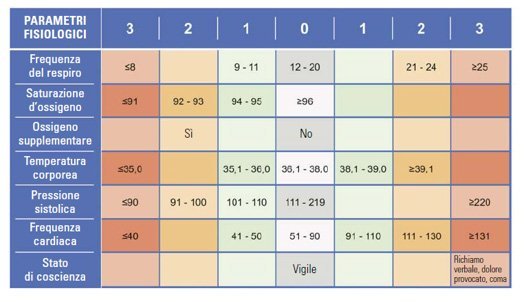
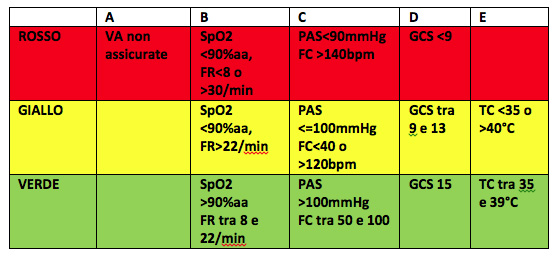
In Pronto Soccorso la prima valutazione del paziente avviene in Triage, dove in base alle alterazioni dei parametri vitali si può attribuire un codice colore per l’ingresso alle sale visita.
|
AIRWAYS Valuto la coscienza; Valuto la capacità di proteggere le vie aeree allineo il paziente e mantengo la pervietà delle vie aeree; Aspiro se necessario; Applico presidi se necessario (cannula oro-rinofaringea) attenzione se riflessi ancora presenti.
|
AIRWAYS IN SEPSI L’alterazione dello stato di coscienza è uno dei parametri vitali rilevabili all’interno del qSOFA;
Valutazione e trattamento sono uguali per tutti i pazienti.
|
|
BREATHING Valuto e osservo il torace;
Osservo tipo di respiro, espansione simmetrica del torace;
Palpo la gabbia toracica; ricerco scrosci, enfisema ecc..;
Ausculto 4 campi polmonari;
Conto la frequenza respiratoria;
Saturimetria;
Somministrare Ossigeno se necessario.
|
BREATHING IN SEPSI eseguo OPACS;
Osservo => respiro di Biot (meningite/encefalite);
Palpo=> enfisema sottocutaneo (germi patogeni, fascite?);
Ausculto => cosa sento?;
C=> FR come criterio qSOFA
S=SPO2;
Emogasanalisi => Rapporto P/F e Lattati.
|
|
CIRCULATION Valuto il polso: frequenza, ritmo, ampiezza;
Valuto parametri quali Tempo di Refill, FC e PA;
Collego il paziente ad un monitor;
Posiziono un accesso venoso del giusto calibro/ eseguo prelievi ematici;
Valuto grosse emorragie/perdite/drenaggi
|
CIRCULATION IN SEPSI Refill come indicatore di ipoperfusione;
Ipotensione come parametro qSOFA;
Penso ad eventuali emocolture;
Infondo Liquidi.
|
|
DISABILITY Eseguo valutazione neurologica del paziente
(GCS o AVPU) o eventuali deficit motori/sensitivi;
Valuto la glicemia;
Valuto la temperatura.
|
DISABILITY IN SEPSI GCS <15 come parametro anomalo valutazione qSOFA.
|
|
EXPOSURE Espongo il paziente ed eseguo una valutazione testa-piede, fronte e retro;
Ricerco ferite, ematomi, segni di venipuntura, fistole, lesioni da pressione, segni di TVP;
Proteggo il paziente dall’ipotermia;
Considero eventuali presidi aggiuntivi
(catetere vescicale per monitoraggio diuresi,
CVC se necessario, SNG).
|
EXPOSURE IN SEPSI Valuto il colore della cute… marezzature?
Giugulari piane o turgide?
Lesioni secernenti?
Sono già presenti accessi vascolari? Stomie? Drenaggi? Catetere vescicale?
Penso ad eventuali colture.
|
Discussion
|
MATERIALE OCCORRENTE |
|
|
PROCEDURA A DUE OPERATORI |
|
PRIMO OPERATORE
SECONDO OPERATORE
|
|
MATERIALE OCCORRENTE PER PRELIEVO DA CATETERE VESCICALE |
|
|
PROCEDURA CON CATETERE VESCICALE |
MOTIVAZIONE SCIENTIFICA |
|
Lavare le mani ed indossare guanti monouso; Clampare con pinza (porre una garza non sterile tra pinza e catetere) o morsetto il catetere 5-10 cm sopra il raccordo con la sacca di raccolta circa 20’-30’; Porre garza sterile con clorexidina al 2% sopra valvola per prelievo (circa per 2’ min), se non presente sraccorda il catetere alla sacca; Aprire il contenitore per esame ponendo attenzione a non toccare la parte interna ed il tappo; Se presente valvola per prelievo aspirare con siringa con inclinazione a 30-45° circa 10 cc di urine, se non presente la valvola porre il contenitore in prossimità dell’estremità del catetere, raccordarlo dalla sacca, sraccordare la pinza il morsetto e raccogliere le urine; Chiudere il contenitore; Applicare l’etichetta. |
Evitare contaminazioni permette la raccolta della diuresi;
Per rimuovere la carica microbica presente impedendo la contaminazione del campione;
Evita la contaminazione del campione.
|
|
MATERIALE OCCORRENTE PER PRELIEVO IN MINZIONE SPONTANEA |
|
|
PROCEDURA IN MINZIONE SPONTANEA |
MOTIVAZIONE SCIENTIFICA |
|
Istruire il paziente sulla modalità di pulizia
Lavarsi le mani
Eseguire un igiene perineale accurata con acqua e detergente: (non utilizzare il disinfettante , potrebbe alterare il campione).
Donna: dall’alto verso il basso;
Uomo: detergere bene il prepuzio.
Aprire il contenitore ponendo attenzione a non toccare la parte interna del tappo e del contenitore;
Tenere a portata di mano il contenitore sterile ed iniziare ad urinare lasciando andare le prime urine nel water/padella;
Raccogliere il mitto intermedio, ponendo il contenitore sotto il flusso urinario, senza toccare con quest’ultimo i genitali esterni in vescica;
Chiudere il contenitore senza toccare il tappo o il suo interno;
Etichettare il campione.
|
Favorisce la corretta esecuzione del campione del meato urinario e di raccolta del campione in modo sterile ed un risparmio economico;
Per evitare contaminazione;
Al fine di rimuovere la flora saprofita presente sulla cute e sulle mucose degli organi genitali esterni;
Si evita la contaminazione del materiale sterile;
Le prime urine lavano il tratto uretrale favorendo il trasporto di secrezioni fuori dal meato;
Nel mitto intermedio l’urina risulta priva di microorganismi presenti nell’uretra o sedimenti;
Al fine di evitare la contaminazione del campione raccolto.
|