- Giuseppe Pepe
- Review
L’approccio ABCDE nello scompenso cardiaco in emergenza urgenza: un nuovo algoritmo decisionale per la gestione clinico/terapeutica
- 1/2017-Febbraio
- ISSN 2532-1285
Giuseppe Pepe(1), Andrea Pavellini(1), Matteo Castelli(1), Simone Vanni(1), Peiman Nazerian(1), Stefano Grifoni(1)
Dipartimento di Emergenza ad Alta Specialità. Medicina e Chirurgia d’Urgenza e Accettazione, Azienda Ospedaliero Universitaria Careggi, Firenze

Introduction
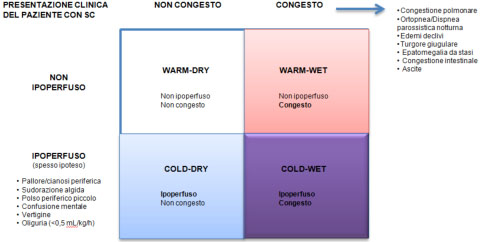
La più eclatante modalità di presentazione dello SC in Pronto Soccorso è l’edema polmonare acuto normo-iperteso (paziente congesto ma non ipoperfuso). Il sintomo cardine è rappresentato dalla dispnea che si aggrava in clinostatismo per il riassorbimento degli edemi declivi e la ridistribuzione del trasudato polmonare dalle basi verso gli apici. Il paziente assume generalmente la posizione seduta (ortopnoica) obbligata, è tachipnoico, confuso, agitato ed ipossico. Può presentare tosse secca o con una modesta quantità di escreato schiumoso e rosato (segno tardivo). Obiettivamente, si apprezzano rantoli più accentuati alle basi ma che nelle forme severe possono interessare tutto l’ambito polmonare; si possono osservare edemi simmetrici degli arti inferiori se allo scompenso sinistro si associa uno scompenso destro. La presenza di pallore, sudorazione fredda e marezzatura cutanea indicano ipoperfusione ed hanno un significato prognostico sfavorevole. Nel contesto dell’edema polmonare, il rilievo di ipotensione è sempre legato alla presenza di una grave problematica miocardica strutturale (es. IMA massivo o complicato da insufficienza mitralica acuta per rottura di corde tendinee o di muscolo papillare); esso si ripercuote pesantemente sia sulle opzioni terapeutiche che sulla prognosi, configurando un quadro di shock cardiogeno.
E’ compito del medico d’urgenza riconoscere l’eziologia dello scompenso cardiaco e ricercare le cause precipitanti, simultaneamente, all’inizio del trattamento specifico, indirizzando il paziente all’adeguato livello di intensità di cure
Valutazione primaria (“Primary Survey”)
Nell’ambito dell’emergenza-urgenza, intra ed extraospedaliera, l’approccio clinico al malato critico con segni e sintomi di SC è in gran parte standardizzato ed organizzato secondo protocolli, in modo tale che possa essere sempre garantita, anche in contesti emotivamente e logisticamente difficili, l’appropriata esecuzione delle manovre necessarie alla stabilizzazione del paziente. Nel primo approccio “frontale” al paziente critico (valutazione primaria – “Primary Survey”), l’iter diagnostico-terapeutico prevede la rapida identificazione delle criticità secondo approccio ABCDE (figura 2) ed eventuale inizio delle manovre di rianimazione (supporto funzioni vitali secondo ACLS (Advanced Cardiac Life Support).
Figura 2.Valutazione primaria
FC = Frequenza cardiaca; PA = Pressione Arteriosa; PV = Parametri Vitali
La verifica della pervietà e la stabilizzazione delle vie aeree (Airway) deve precedere qualsiasi intervento rianimatorio, comprendente l’ispezione dell’area del collo e della trachea (trachea in asse, giugulari turgide), seguita poi dalla valutazione e stabilizzazione della funzione respiratoria (Breathing) e quindi dell’emodinamica (Circulation). Si sottopone il paziente a monitoraggio ECG e dei parametri vitali; si somministra ossigeno supplementare secondo device opportuno (bassi flussi, Venti-mask, alti flussi + reservoir 12-15 l/min) se la saturazione è inferiore al 90%. In seguito dovrà essere valutata la presenza di danno neurologico o disabilità (Disability) e il paziente dovrà essere valutato nel suo insieme (Exposure) per individuare la presenza di altri tipi di lesione non direttamente compromettenti i parametri vitali.
Approccio diagnostico (“Diagnostic Survey”)
L’approccio diagnostico al paziente con sospetto scompenso cardiaco deve essere iniziato in ambiente pre-ospedaliero da parte del servizio di emergenza territoriale e poi continuato nel dipartimento di emergenza, in modo da definire precocemente il quadro clinico del paziente (inquadramento diagnostico e diagnosi differenziale) per iniziare il trattamento specifico ed arrestare un processo possibilmente evolutivo.
In emergenza urgenza il medico può seguire un approccio mnemonico sequenziale secondo lo schema ABDCE (figura 3):
- A.ANAMNESI – L’anamnesi viene generalmente condotta in parallelo con le prima manovre di stabilizzazione ed è fondamentale per il corretto inquadramento del paziente e per la diagnosi differenziale con sindromi dispnoiche di altra origine (asma, riacutizzazione di BPCO, versamento pleurico, polmonite, pneumotorace, embolia polmonare, intossicazioni, malattie neuromuscolari, attacco di panico) e sindromi edemigene (insufficienza venosa, farmaci, ipoproteinemia, insufficienza epatica, insufficienza renale, sindrome nefrosica, linfedema). Devono essere indagati tempi e modalità di insorgenza della dispnea (classe funzionale NYHA), eventuali sintomi associati (febbre, dolore toracico, cardiopalmo); deve essere ricercata la presenza nell’anamnesi personale di cardiopatie, ipertensione arteriosa, diabete mellito, distiroidismi, esposizione a farmaci cardiotossici o trattamento radiante.
- B.BLOOD TEST (valuta NT-proB e concomitante prelievo ematico per esami di laboratorio (raccomandati glucosio, emocromo, elettroliti sierici, creatininemia, bilirubina, ALT), valutando il dosaggio del D-dimero (nel sospetto di embolia polmonare, del TSH e del Peptide Natriuretico (BNP o pro-BNP). Quest’ultimo, seppur esame costoso, può essere utilizzato per la diagnosi differenziale della dispnea: nel caso in cui il valore di BNP sia inferiore a 100 pg/mL o NT-proBNPinferiore a 300 pg/mLla diagnosi di SC è improbabile; valori di NT-proBNP superiori a 300 pg/mL, soprattutto in associazione ad anomalie del tracciato elettrocardiografico rafforzano il sospetto di SC e rendono necessaria l’esecuzione di un SCA, embolia polmonare e ipertensione polmonare, miocarditi, tachiaritmie atriali e ventricolari, età avanzata, insufficienza renale, cirrosi epatica, anemia e infezioni severe (polmoniti e sepsi).
- C.CARDIOPATIA ISCHEMICA – Verifica SCA o storia di cardiopatia ischemica. Si esegue un ECG a dodici derivazioni (alto valore predittivo negativo) per evidenziare la presenza di alterazioni di tipo ischemico, aritmiesegni di cardiopatia strutturale quali dilatazione atriale, ipertrofia-sovraccarico ventricolare. Nel caso di sospetta genesi ischemica dello SC è possibile dosare i marcatori biochimici miocardio-specifici
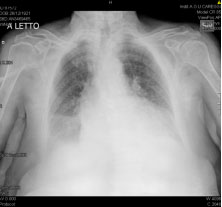
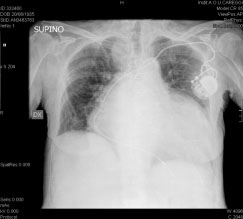
- D.DISFUNZIONE VS (ventricolo sinistra) – Approccio ecografico cardio-toracico bed side (I livello) consente al medico dell’urgenza di valutare in tempi rapidi l’aspetto complessivo del cuore, le dimensioni e la cinetica delle camere cardiache, la presenza di valvulopatie, trombosi, dissecazione aortica versamento pericardico, le dimensioni e la compliance respiratoria della vena cava inferiore, l’ecostruttura polmonare (linee B in caso di edema interstiziale), la presenza di versamento pleurico e di segni che orientino verso altre cause di dispnea (pneumotorace, addensamenti di natura infiammatoria o infartuale, atelettasie).
- Nelle forme di SC con prevalente disfunzione sistolica si ha una dilatazione del ventricolo sinistro con ipocinesia parietale e riempimento cons
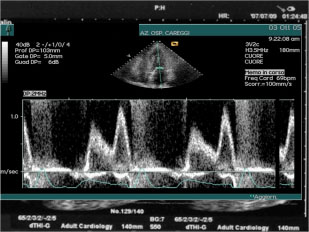
- Nelle forme prevalentemente diastoliche le dimensioni del ventricolo sinistro sono normali e la FE può essere normale o solo lievemente ridotta, ma il riempimentdiastolico è alterato. Questo fenomeno è apprezzabile allo studio eco Doppler del flusso trans-). La disfunzione diastolica si osserva frequentemente nel contesto della cardiopatia ischemica perché il rilasciamento ventricolare è un processo attivo, energia-dipendente; inoltre il sovraccarico cronico di pressione e/o di volume conducono ad un rimodellamento miocardico che comporta un aumento della rigidità di parete.
- In molti casi lo SC è caratterizzato dalla co-esistenza di disfunzione sistolica e diastolica.
- E.EMOGASANALISI ARTERIOSA / II tipo o globale se concomitante incremento della pCO2>45mmHg) e la necessità di O2-terapia indirizzando il medico d’urgenza sul tipo di presidio da utilizzare; permette di valutare l’equilibrio acido-base (possibile acidosi metabolica iperlattacidemica, acidosi respiratoria e relativo . In caso di segni di ipoperfusione periferica o di indicazione a trattamento con NIV vi è indicazione al cateterismo arterioso per il monitoraggio invasivo della pressione arteriosa e per la ripetizione periodica di EGA.
Altri esami diagnostici
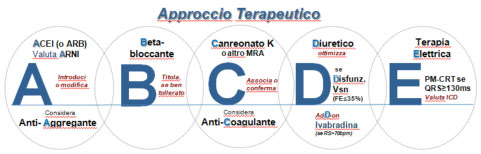
Approccio terapeutico (“Therapeutic Survey”)
- SCA (indicazione a tentativo di rivascolarizzazione percutanea entro 2 ore dall’accesso in ospedale)
- emergenza ipertensiva (il target terapeutico iniziale è rappresentato da una riduzione della pressione arteriosa del 25% durante le prime ore con vasodilatatori in associazione con diuretici dell’ansa per via endovenosa)
- aritmie (in caso di instabilità emodinamica vi è indicazione a cardioversione elettrica o pacing altrimenti possibilità di terapia medica)
- causa meccanica acuta complicante SCA (rottura di parete libera del ventricolo sinistro, difetto interventricolare, insufficienza mitralica acuta), trauma cardiaco, insufficienza valvolare acuta secondaria a endocardite, dissecazione aortica (valutare indicazione a trattamento cardiochirurgico)
- tromboembolia polmonare (in caso di instabilità emodinamica vi è indicazione a somministrazione di eparina non frazionata per via endovenosa seguita dalla trombolisi sistemica, se vi sono controindicazioni alla trombolisi possono essere valutate l’embolectomia trans catetere o la trombo-endoarterectomia polmonare chirurgica in emergenza).
- riduzione della dispnea
- mantenimento di una saturazione arteriosa dell’ossigeno (SpO2) > 92%
- mantenimento di una pressione arteriosa media (PAM) di almeno 65 mm Hg
- riduzione della frequenza cardiaca
- mantenimento di una diuresi > 0,5 mL/kg/h (deve essere predisposto un controllo della diuresi, se necessario mediante cateterismo vescicale).
- prevenzione o almeno limitazione del danno cardiaco e renale secondario.
- A.ACE inibitore (Angiotensin-Converting Enzyme Inhibitor, ACEI), in tutti i pazienti sintomatici con frazione d’eiezione ridotta in associazione a terapia Beta-bloccante. Nei pazienti intolleranti per tosse l’ACE inibitore può essere sostituito da un antagonista del recettore AT1 (Angiotensin II Receptor Blocker, ARB); tuttavia, ACE inibitori e ARB condividono gran parte delle controindicazioni (gravidanza, storia di angioedema, stenosi bilaterale delle arterie renali o monolaterale in monorene anche funzionale).
- B.Beta-bloccante, in tutti paziente con SC stabile riduce il rischio di mortalità e ospedalizzazione (controindicato in caso di BAV avanzato ed asma grave) da iniziare a basso dosaggio e titolare fino alla dose “target” o fino alla dose massima tollerata; se la terapia con beta-bloccante è già in corso non è necessario sospenderla durante la riacutizzazione di SC.
- C.Canrenoato di potassio
- D.Diuretici (dell’ansa e tiazidici) per alleviare segni e sintomi di congestione (non riducono il rischio di ospedalizzazione o morte), in acuzie vengono titolati/ottimizzati anche sulla base del profilo emodinamico: l’aggiustamento posologico deve essere effettuato sulla base del monitoraggio dei segni e sintomi di congestione, dei valori di pressione arteriosa e sulla misura quotidiana del peso corporeo. Il trattamento con diuretici e con ACE inibitori o sartani deve sempre essere condotto con attenzione alla funzionalità renale e agli elettroliti.
- E.Terapia Elettrica. Nei pazienti che rimangono sintomatici (classe NYHA II-IV) e in cui, nonostante la terapia farmacologica ottimale, persista una FE ≤ 35% vi è indicazione ad impianto di PM biventricolare con funzione di resincronizzazione cardiaca (CRT) se presenza di ritmo sinusale e durata del QRS ≥ 130 ms.
Esito (“Outcome”)
- insufficienza renale con azotemia > 43 mg/dL e/o creatinina > 2,75 mg/dL
- la pressione arteriosa sistolica minore di 115 mm Hg
- l’aumento della troponina I cardiaca.
- diagnosi nota di SC
- stabilità emodinamica e respiratoria
- PAS di 100-120 mm Hg alla presentazione
- non necessità in acuto di farmaci vasoattivi
- frequenza respiratoria< 32/min
- non necessità in acuto di NIV
- assenza di nuove alterazioni ECG
- valori normali di troponina
- azotemia < 40 mg/dL
- creatinina < 3 mg/dL
- iniziale risposta positiva alla terapia in acuto (in termini di clinica e diuresi)
- assenza di significative comorbilità richiedenti trattamento attivo
- adeguata compliance, supporto familiare e possibilità di follow up.
- miglioramento clinico (riduzione della dispnea, della frequenza respiratoria, dei reperti obiettivi anche durante attività
- identificazione e trattamento, anche parziale, del fattore precipitante
- non alterazioni significative degli esami ematici (in primis funzionalità renale ed elettroliti)
- rivalutazione ecografica della FE eseguita in osservazione o programmata in tempi brevi
- transizione alla terapia diuretica orale per almeno 24-48 ore
- adeguata impostazione della terapia a lungo termine
- programmazione di adeguato follow up a 7-10 giorni
- adeguata compliance e support familiare
- adeguata educazione del paziente riguardo alla dieta, al fumo, ai farmaci, al peso corporeo, alle vaccinazioni e al riconoscimento di segni e sintomi che richiedono una rivalutazione medica.
Conclusioni
Viene proposto un veloce algoritmo decisionale ABCDE, sequenziale, che dovrebbe aiutare mnemonicamente il medico di emergenza urgenza nelle fasi del percorso diagnostico/terapeutico del paziente con segni e sintomi secondari a scompenso cardiaco acuto e cronico, tenendo conto delle indicazioni provenienti dalle Linee Guida internazionali in tema di diagnosi e terapia del paziente con scompenso cardiaco.
Letture consigliate
– 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC)Developed with the special contribution of the Heart Failure Association (HFA) of the ESC.. Eur Heart J. 2016 Jul 14;37(27):2129-200.
– 2016 ACC/AHA/HFSA Focused Update on New Pharmacological Therapy for Heart Failure: An Update of the 2013 ACCF/AHA Guideline for the Management of Heart Failure: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Failure Society of America. J Card Fail. 2016 Jul 6. pii: S1071-9164(16)30550-4.